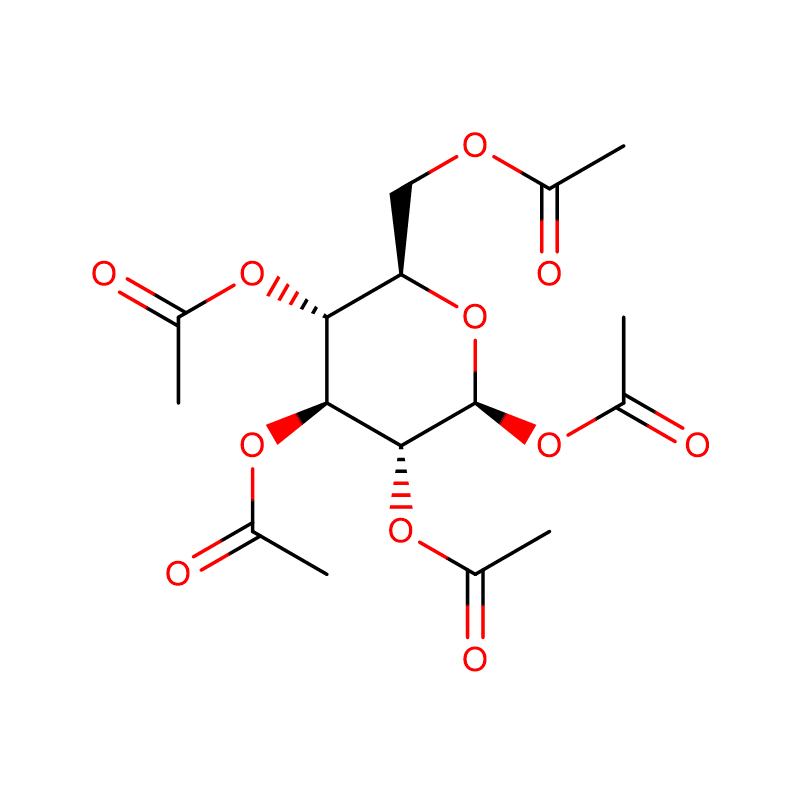
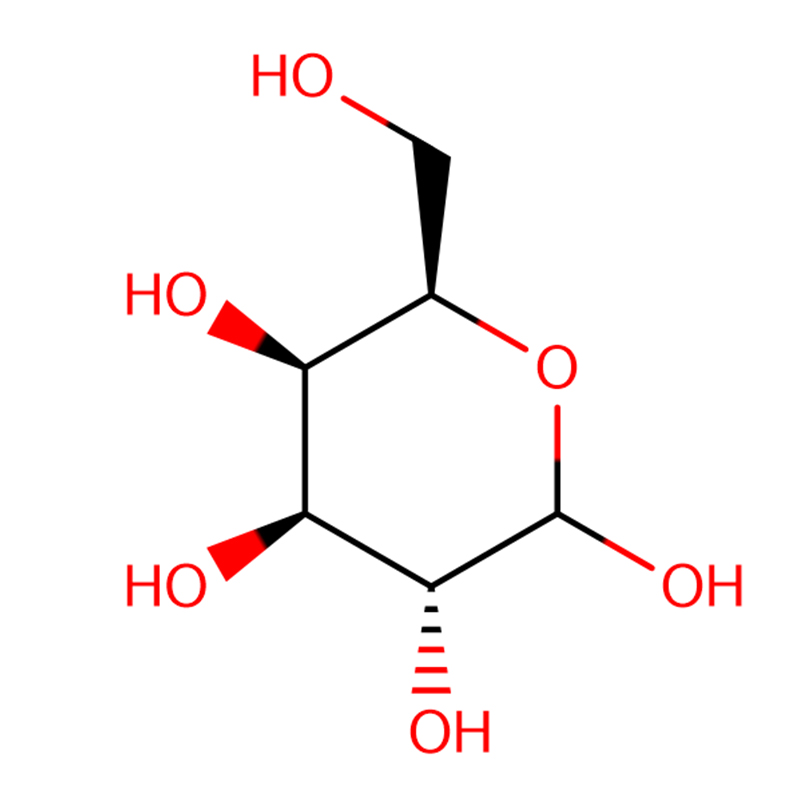
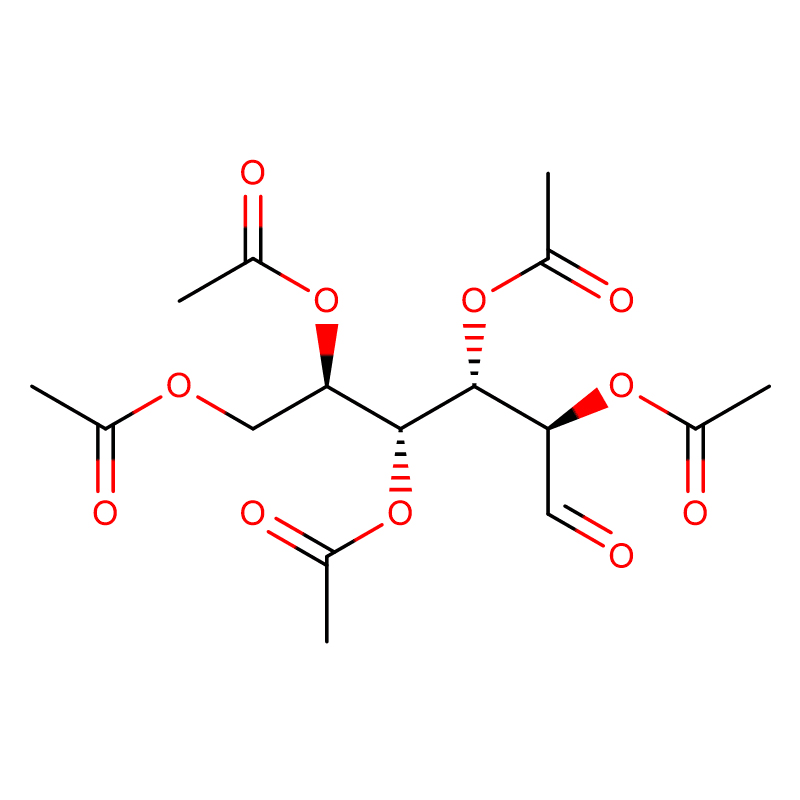
4-NITROPHENYL-ALPHA-D-MANNOPYRANOSIDE CAS:10357-27-4 Off-White Pudder 98%
| Katalognummer | XD90011 |
| Produit Numm | 4-Nitrophenyl-alpha-D-mannopyranoside |
| CAS | 10357-27-4 |
| Molekulare Formel | C12H15NO8 |
| Molekulare Gewiicht | 30301.25 |
| Stockage Detailer | -2zu -8°C |
| Harmoniséierten Tarifcode | 29400000 |
Produit Spezifizéierung
| Waasser | <5% Karl Fische |
| Solubilitéit | 1% an DMF ass kloer a faarweg |
| Rengheet | Gratis 4-Nitrophenol <200ppm |
| HPLC | >98% |
| Ausgesinn | Off-wäiss Pudder |
Mechanesch Abléck an eng Ca2+-ofhängeg Famill vun Alpha-Mannosidasen an enger mënschlecher Darm Symbiont.
Colonic Bakterien, illustréiert duerch Bacteroides thetaiotaomicron, spillen eng Schlësselroll fir d'mënschlech Gesondheet z'erhalen andeems se grouss Famille vu Glykosidhydrolasen (GHs) ausnotzen fir Diät-Polysacchariden an Host-Glykanen als Nährstoffer auszenotzen.Esou GH Famill Expansioun ass illustréiert vun der 23 Famill GH92 Glykosidasen kodéiert vum B. thetaiotaomicron Genom.Hei weisen mir datt dëst Alpha-Mannosidasen sinn déi iwwer en eenzegen Verschiebungsmechanismus handelen fir Host N-Glykanen ze benotzen.Déi dreidimensional Struktur vun zwee GH92 Mannosidasen definéiert eng Famill vun zwee-Domain Proteinen, an deenen de katalytesche Zentrum um Domain Interface läit, wat Säure (Glutamat) a Base (Aspartat) Hëllef zur Hydrolyse an engem Ca(2+)- ofhängeg Manéier.Déi dreidimensional Strukture vun den GH92s a Komplex mat Inhibitoren bidden Abléck an d'Spezifizitéit, de Mechanismus an d'Konformatiounsroute vun der Katalyse.Ca(2+) spillt eng wichteg katalytesch Roll bei der Verzerrung vum Mannoside ewech vu sengem Grondzoustand (4)C(1) Stullkonformatioun an den Iwwergangszoustand.(Bibliographie: Nat.Chem.Biol.6, 125-32, (2010)
Frontal Affinitéitschromatographie vun Ovalbumin Glycoasparaginen op enger Concanavalin A-Sepharose Kolonn.Eng quantitativ Studie vun der Bindungsspezifizitéit vum Lektin.
D'Interaktioune vu Sepharose 4B-immobiliséierter concanavalin A (ConA) mat 10 Glycoasparaginen ofgeleet aus ovalbumin goufen quantitativ duerch frontal Affinitéitschromatographie ënnersicht.An dëser Method gëtt eng Kohlenhydratléisung kontinuéierlech op eng ConA-Sepharose Kolonn applizéiert an d'Verzögerung vun der Elutiounsfront gëtt als Parameter vun der Stäerkt vun der Interaktioun gemooss.D'Dissoziatiounskonstant (Kd) fir all Saccharid mat ConA ka bestëmmt ginn.Eng Analyse vun der Bindung vu p-nitrophenyl-alpha, D-mannoside huet gewisen datt d'bindende Eegeschafte vu ConA net wesentlech änneren no der Immobiliséierung op Sepharose 4B.Jiddereng vun den ovalbumin glycoasparagines war mat Tritium vun der reductive methylation Method fir Analyse markéiert.E Verglach vun de kritt Kd Wäerter huet gewisen datt d'Bindung vu ConA wesentlech variéiert mat ganz liichte strukturellen Differenzen vun der Glykosylkette.D'Resultater suggeréieren datt ConA eng spezifesch Glykosylkettestruktur erkennt, Man alpha 1-6 (Man alpha 1-3) Man, an där op d'mannst eng Hydroxylgrupp op der C-3 Positioun vun der C-6-verbonne Mannose fräi soll sinn.